Association d’un agent antipaludéen et d’un produit issu du microbiote intestinal pour le traitement des cancers primitifs du foie
Par le Professeur Jamila FAIVRE, Directrice de recherche, Unité INSERM UMR 1193, Microbiote, inflammation et cancer, Université Paris Saclay, AP-HP Hôpital paul Brousse, Centre hépato billiaire, Villejuif

Le cancer primitif du foie est l’un des cancers les plus fréquents dans le monde. Il comprend le carcinome hépatocellulaire (CHC) et le cholangiocarcinome intrahépatique (ICC).
En 2018, il était la deuxième cause de mortalité liée au cancer chez l’homme et la quatrième chez la femme.
Le CHC représente 80% des cas de cancer primitif du foie ; il se développe habituellement sur une cirrhose et est souvent diagnostiqué à un stade avancé de la maladie. Les causes du CHC sont multiples ; les infections virales par les virus des hépatites B et C, l’alcool, la stéato-hépatite non alcoolique (NASH) des obèses, et le syndrome métabolique sont des causes majeures de CHC.
L’incidence annuelle du CHC est en très forte augmentation au cours des 20 dernières années. Le pronostic est sévère (taux de survie à 5 ans < 10%) en l’absence de greffe de foie réalisée chez 3 à 4% des patients (pénurie de greffons, inéligibilité des patients avec cancer avancé) avec des taux de survie globale à 5 ans de 60-80% et des taux de récidive tumorale de 5-20%. La résection chirurgicale et les techniques d’ablation locale sont souvent associées à des récidives tumorales (taux de survie sans récidive à 5 ans de 65%).
L’efficacité des agents de chimiothérapie, des thérapies ciblées et de la radiothérapie est limitée en termes de survie, d'où l'urgence de développer de nouvelles stratégies thérapeutiques.
La recherche de nouvelles stratégies thérapeutiques :
Nous sommes partis de l’hypothèse suivante : L'autophagie est un processus physiologique fondamental de survie et d’homéostasie cellulaires hautement régulé. L'autophagie est activée ou inhibée dans de nombreux états pathologiques incluant les organes cancéreux, et joue un rôle double selon le stade de développement du cancer, son type et son microenvironnement. Selon sa fonction (suppresseur de tumeur ou oncogène), les voies de l’autophagie sont considérées comme des cibles potentielles dans le traitement du cancer et l’amélioration de la réponse aux traitements anticancéreux standards, bien que peu de composés manipulant le processus autophagique aient été caractérisés.
Parmi les méthodes ciblant la machinerie autophagique, son activation et blocage simultanés, seuls ou en combinaison avec la chimiothérapie, est une approche particulièrement intéressante faisant passer l'autophagie du stade de cytoprotection à celui de cytotoxicité.
Notre projet a porté sur l’évaluation préclinique de l’activité anti-tumorale et le mécanisme d’action d’une combinaison associant la chloroquine et le butyrate. Le butyrate, un métabolite issu du microbiote intestinal connu pour être un activateur de l’autophagie et la chloroquine, un agent antipaludéen inhibiteur de l’autophagie, pourraient agir en synergie pour induire la mort de cellules cancéreuses. Ainsi, dans la présente étude, nous avons exploré le mécanisme de chaque composé individuel et leur action combinée.
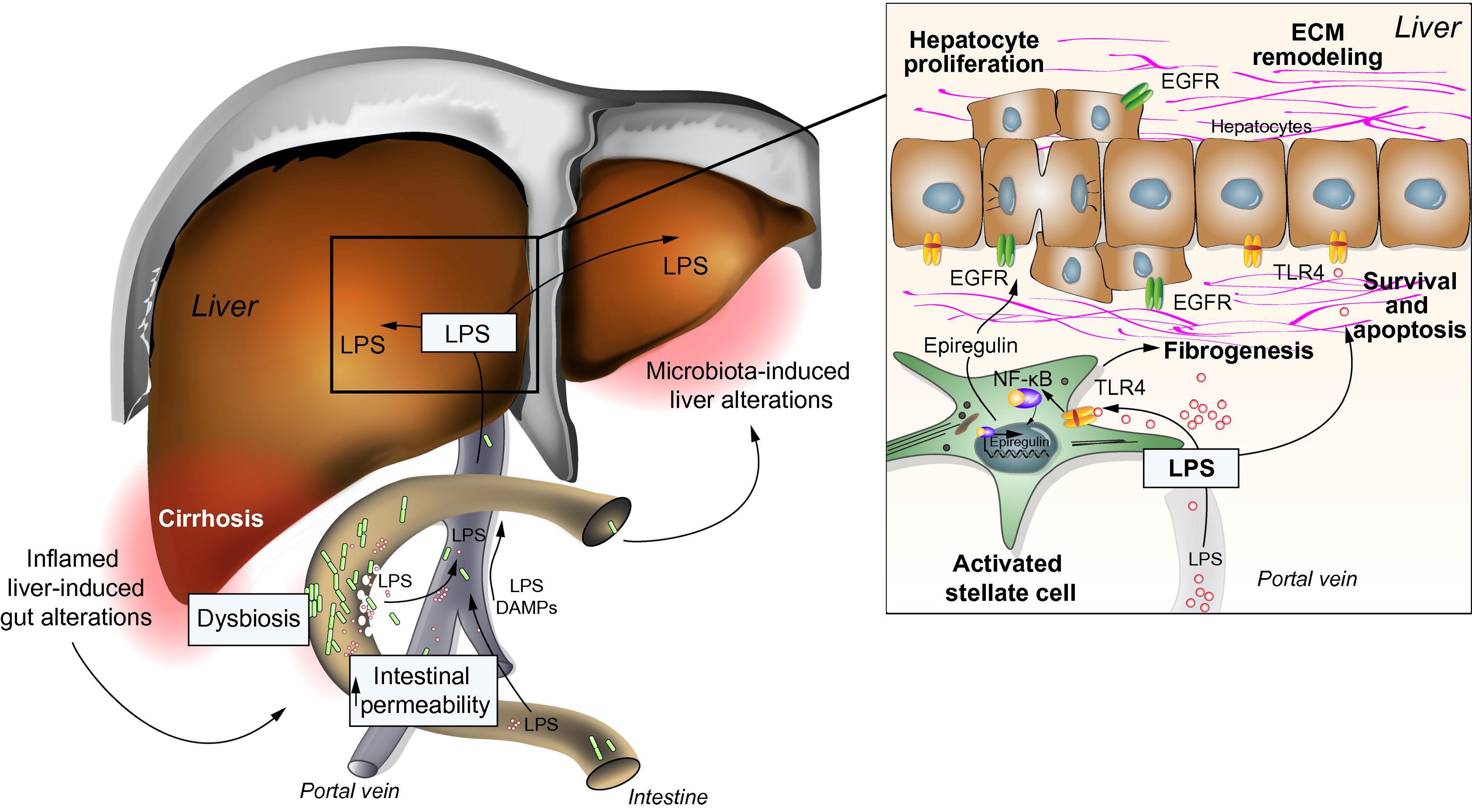
Les résultats obtenus
combinaison du butyrate et de la chloroquine agissent en synergie pour induire une mort apoptotique prononcée de nombreuses lignées cellulaires humaines dérivées de CHC et de ICC.
Nous notons une absence de cytotoxicité dans des hépatocytes primaires humains normaux indiquant une action spécifique sur les cellules cancéreuses. Nous montrons que le butyrate favorise la synthèse d’autophagosomes et que la chloroquine bloque la dernière étape du processus d'autophagie, ce qui entraine une accumulation accrue d'autolysosomes.
Il en résulte une accumulation d'autolysosomes altérés, une augmentation des niveaux d'espèces réactives de l'oxygène (ROS), une induction de la perméabilisation de la membrane du lysosome (LMP) et une libération de cathepsines dans le cytosol.
En conclusion : dans l'ensemble, notre étude montre que l'induction et le blocage simultanés de l'autophagie est une stratégie prometteuse pour le traitement des cancers primitifs du foie. Nos résultats suggèrent que cette stratégie est une approche thérapeutique puissante de lutte contre ces cancers, et ce quel que soit le degré d’induction endogène de l’autophagie, et que les produits dérivés du microbiote améliorent la sensibilité des cellules cancéreuses du foie aux agents anti-tumoraux.
Présentation de l'unité INSERM UMR 1193 Microbiote, inflammation et cancer
Le Professeur Jamila Faivre est Docteur en médecine et Professeur des Universités en Biologie Cellulaire à l’Université Paris-Saclay et à l’UFR de médecine où elle enseigne la biologie cellulaire et l’oncologie. Elle dirige une équipe INSERM intitulée “Microbiote, Inflammation et Cancer” au sein de l’unité mixte de recherche U1193 / Université Paris-Saclay dans le Centre Hépatobiliaire de l’hôpital Paul-Brousse, centre expert des maladies du foie et de la transplantation. Son activité hospitalière de biologie spécialisée se déroule dans le laboratoire d’Oncogénétique moléculaire et cytogénétique labélisée par l’INCa pour le diagnostic et le traitement personnalisé des cancers hématologiques du territoire Paris Sud.
Les activités hospitalo-universitaires du Professeur Jamila Faivre relèvent de la biologie cellulaire dans ses aspects physiopathologiques et d’innovations diagnostiques et thérapeutiques. Elle associe une recherche fondamentale à une recherche translationnelle dans les domaines de l’oncologie et des maladies inflammatoires chroniques. Les questions scientifiques abordées par l’équipe du Professeur Faivre sont centrées sur les interactions hôte-microbes, l’axe intestin - foie, l'immunité innée (peptides antimicrobiens), le microbiote intestinal, et le rôle des stress oxydatif et inflammatoire dans les maladies inflammatoires chroniques et la carcinogenèse. Les thématiques de recherche de l’équipe Faivre qui portent sur l'exploration des activités biologiques du microbiote intestinal en relation avec l’inflammation et la carcinogenèse et le développement de nouvelles approches thérapeutiques ciblant le microbiote intestinal s’inscrivent dans des thématiques centrales pour la recherche biologique et médicale. Plus précisément, les axes de recherche de l'équipe sont (i) la compréhension des mécanismes de cross-talk entre bactéries commensales et cellules épithéliales; (ii) l'étude du rôle des peptides et protéines antimicrobiens dans la régulation du microbiote intestinal et la robustesse de la barrière intestinale; (iii) l'identification de signatures de microbiomes associées à des états pathologiques ainsi que la compréhension des liens fonctionnels entre microbiotes dysbiotiques et maladies tumorales; (iv) le développement d’approches thérapeutiques nouvelles capables de prévenir ou d’améliorer des maladies chroniques communes associant une dysbiose intestinale au moyen de la pharmacobiotique et de la thérapie biologique.
